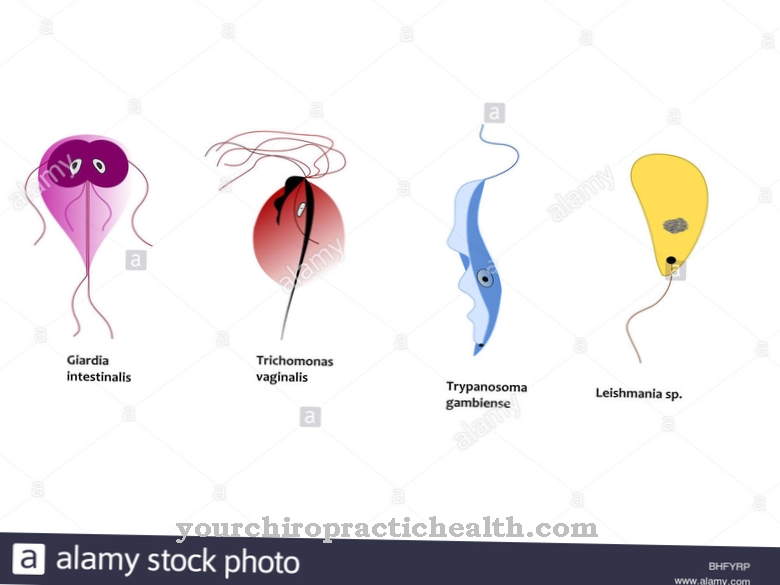
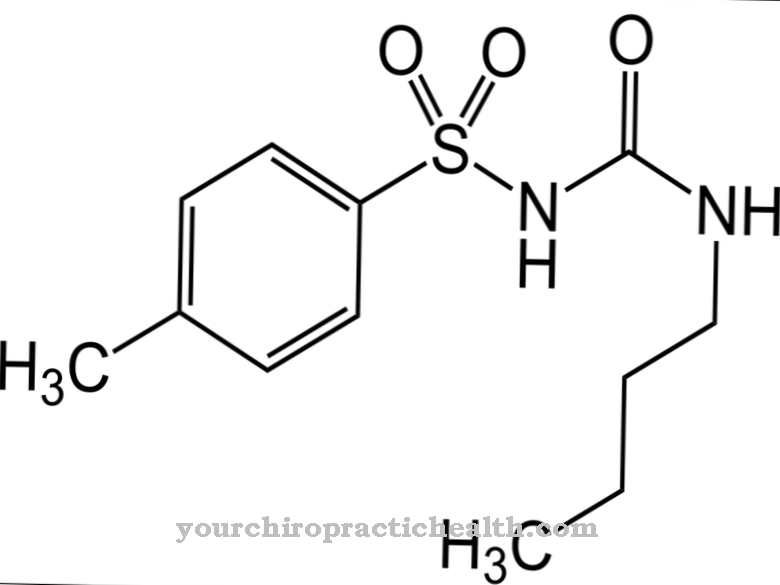
З осмотичний тиск відповідає тиску, який присутній у розчиннику на більш висококонцентрованій стороні напівпроникної або селективно проникної мембрани. Тиск рухає потоком розчинника через мембрану і диктує його напрямок. Захворювання, пов'язані з осмотичним тиском, це, наприклад, знижена стійкість до тиску клітин крові.
Що таке осмотичний тиск?

Терміном осмотичний тиск медицина описує фізіологічний тиск, що дає можливість осмосу. Осмоз відповідає направленому потоку молекулярних частинок через напівпроникні або селективно проникні розділяючі шари. Це означає, що осмос - це важливий транспорт речовин в організмі людини.
Осмотичний тиск - головна вимога цього процесу масообміну. Розчинені молекули у розчиннику викликають осмотичний тиск на стороні поверхні з більшою концентрацією. Отримані в результаті співвідношення тиску подають потік розчинника через відповідну мембрану. Таким чином розчинник переміщується з боку з нижчою концентрацією частинок через мембрану і, таким чином, стікає в бік з більшою концентрацією, в якій існує осмотичний тиск. Самі молекулярні частинки не можуть пройти через напівпроникну або селективно проникну мембрану.
Функція та завдання
Осмотичний тиск залежить від співвідношення концентрацій двох розчинів, які розташовані з різних сторін напівпроникної або селективно проникної мембрани. Хоча існує осмотичний тиск на нижній концентрованій стороні, тиск завжди вище на більш концентрованій стороні розчиненого речовини.
В організм людини вода потрапляє в окремі клітини з інтерстицію. Цей приплив відбувається з боку з меншою концентрацією в сторону з більш високою концентрацією. Клітини мають певний внутрішній тиск. Цей тиск також відомий як тургор. Приплив триває до тих пір, поки тургор у клітинах не досягне того ж рівня, що й осмотичний тиск. Отже, тиск, що існує зсередини, і тиск, що діє зовні, є еквівалентними в кінці припливу.
Осмотичний тиск можна виміряти та обчислити. У принципі ті ж закони фізики застосовуються в розведених рідких розчинах, як і в ідеальних газах. З цієї причини осмотичний тиск у кожному випадку завжди пропорційний абсолютній температурі. Крім того, існує пропорційність між молярною концентрацією конкретної розчиненої речовини та рівнем осмотичного тиску.Тиск залежить насамперед від кількості молекулярних частинок у розчиненій речовині.
У розчині одного моля речовини в 22,4 л розчинника осмотичний тиск при температурі 0 градусів Цельсія або 273,15 Кельвіна становить 101,325 кПа. Закон Ван-не Гоффа забезпечує ці відносини. Однак закон застосовується лише до розведених розчинів нижче значення 0,1 М.
Аналогія законам ідеальних газів полягає в наступному: осмотичний тиск протидіє припливу розчинників. З цієї причини приплив розчинника припиняється, як тільки досягається рівновага.
Осмотичний тиск розчину можна визначити за допомогою осмометрів. Тиск вимірюється або статично, після досягнення рівноваги, або динамічно. При динамічному вимірюванні для манометра стояка необхідно подати зовнішній тиск, щоб перервати осмотичний потік. За допомогою вимірювання тиску можна також визначити середню молекулярну масу макромолекул.
Хвороби та недуги
Наприклад, захворювання, пов'язані з осмотичним тиском, можуть вражати клітини крові. Еритроцити мають осмотичну стійкість. Ця осмотична стійкість еритроцитів знижується при різних захворюваннях. Так само, як багато захворювань пов’язано із збільшенням осмотичної резистентності. Для розпізнавання таких захворювань вимірюють осмотичну резистентність еритроцитів. Передусім, вимірювання дає можливість діагностувати резистентні захворювання.
До таких захворювань можна віднести, наприклад, сфероїдну клітинну анемію. Однак інші гемолітичні анемії також можуть знизити осмотичну стійкість еритроцитів. Гемолітична анемія - це група захворювань, пов’язаних з анемією внаслідок збільшення або передчасного розпаду еритроцитів. Медицина називає цей факт гемолізом. Гемоліз часто пов’язаний з основними захворюваннями. Вони можуть бути викликані механічними процесами або генетичним диспозицією. Крім фізіологічного гемолізу внаслідок віку еритроцитів, руйнування може визначати механічне надмірне використання, таке як заміна серцевого клапана, термічні пошкодження від нагрівання та осмотичні пошкодження. У разі осмотичного пошкодження гіпер- або гіпоосмолярні розчини є фактичною причиною занепаду.
Для вимірювання осмотичної резистентності еритроцити пацієнта поміщають у пробірки зі збільшенням концентрації солі. В одній з трубок міститься майже чиста вода. Одна містить концентрацію солі, яка оптимальна для еритроцитів. Через 24 години клітини крові лопаються в чистій воді. У пробірках з більш високою концентрацією солі розривається лише декілька клітин крові. Якщо хворий страждає захворюванням зі зниженою осмотичною стійкістю клітин крові, тільця лопаються навіть у більш високих концентраціях солі і не можуть протистояти осмотичному тиску.
Осмотичний опір також можна збільшити. Підвищення стійкості неспецифічне і може бути наслідком різних захворювань. Прикладами захворювань із підвищеною осмотичною стійкістю еритроцитів є таласемія, залізодефіцитна анемія та серповидноклітинна анемія. Крім того, жовтяниця та ураження печінки можуть підвищити опірність.







.jpg)